Spre deosebire de nanosistemele artificiale, sistemele biologice sunt în așa fel concepute încât, în mod ideal, să răspundă la necesitățile și reacțiile mediului intern. În această privință, diferite tampoane moleculare naturale asigură livrarea cantitativă cu precizie a unor molecule specifice, prin mecanisme autoreglate, bazate pe principiul lui Le Chatelier („legea echilibrului chimic”). Într-un studiu, un grup de cercetători a aplicat principiul lui Le Chatelier, proiectând tampoane moleculare autoreglate de ADN pentru medicamentul chimioterapeutic doxorubicină și agentul antimalarie numit chinină. Ei au demonstrat faptul că tampoanele pe bază de aptameri (adică secvențe scurte de ADN sau ARN sintetic, care leagă o moleculă țintă specifică) au capacitatea de a fi programate pentru a menține orice concentrație specifică dorită medicamentului liber, în studii atât in vitro, cât și in vivo, ceea ce permite optimizarea stabilității chimice, coeficientului de partiție, a farmacocineticii și a biodistribuției medicamentului. De asemenea, au demonstrat că aceste „tampoane programabile” pot fi construite din orice polimer, iar utilizarea lor ar trebui să îmbunătățească rezultatele terapeutice, atât prin creșterea bioactivității medicamentului, cât și prin minimizarea efectelor adverse și a frecvenței de dozare.
Noua clasă de nanotransportori a fost concepută și validată de către o echipă de cercetători de la Universitatea din Montreal, prezentându-și rezultatele într-un studiu publicat în revista Nature Communications. Utilizarea nanotransportorilor pe bază de ADN , care sunt de 20.000 de ori mai mici decât un fir de păr al unui om, ar putea îmbunătăți semnificativ protocoalele de terapie și profilaxie ale cancerului și ale altor boli. Furnizarea și menținerea unei doze terapeutice corespunzătoare dintr-un anumit medicament, pe tot parcursul unui tratament, este una dintre modalitățile cheie de a trata boala respectivă cu succes. Supraexpunerea la o anumită medicamentație poate avea efecte adverse dintre cele mai neplăcute și, pe de altă parte, expunerea terapeutică subliminală poate duce nu doar la reducerea eficienței terapeutice, dar și la rezistența la medicamente. În medicina de azi, o provocare majoră este menținerea unei concentrații optime de medicamente în sânge. Întrucât majoritatea medicamentelor se degradează rapid, pacienții sunt nevoiți să ia doze multiple, asta la intervale regulate.
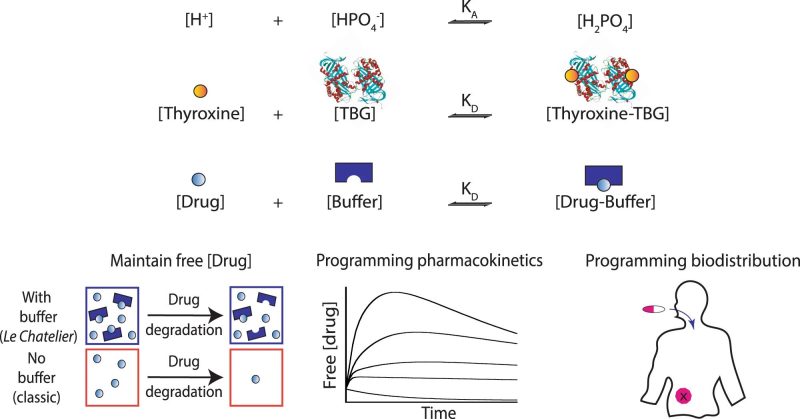
Implicit, mulți pacienți uită adesea să-și administreze medicamentația la timp, iar acest lucru se traduce prin o dozare mai mică decât cea corespunzătoare, optimă. Mai mult decât atât, toți pacienții au un profil farmacocinetic distinct, unic, concentrația medicamentului în sânge fiind, de asemenea, diferită. Observând că doar aproximativ 50% dintre pacienții cu cancer primesc o doză optimă de medicament în timpul anumitor protocoale chimioterapeutice, un profesor de chimie de la UdeM, Alexis Vallée-Bélisle, expert în biotehnologii, a început să exploreze atent modul în care sistemele biologice controlează și mențin concentrația de biomolecule. „Astfel, am descoperit că organismele vii folosesc transportori de natură proteică ce sunt programați să mențină concentrația precisă a unor molecule cheie, cum ar fi hormonii tiroidieni, și că puterea interacțiunii dintre acești transportori și moleculele lor dictează concentrația precisă, exactă, a moleculei libere”, a declarat el.
Această descoperire l-a determinat pe Alexis Vallée-Bélisle, expert în domeniul bioingineriei și bionanotehnologiei, și pe echipa sa de cercetare, să dezvolte transportori artificiali, sintetici, de medicamente, care imită efectul natural și fiziologic de menținere a unei concentrații exacte a unui medicament în timpul tratamentului. Arnaud Desrosier, doctorand, precum și principalul autor al studiului, a identificat și dezvoltat, inițial, doi transportori de ADN: unul pentru chinină și celălalt pentru dexorubicină, medicamentul utilizat în mod obișnuit pentru tratarea leucemiei și melanomului. El a demonstrat apoi că acești transportori artificiali pot programați ușor pentru a furniza și menține orice concentrație specifică a unui anumit medicament.
„Mai interesant este faptul că, de asemenea, am descoperit că acești nanotransportori ar putea fi utilizați și «rezervoare de medicamente», pentru a prelungi efectul acestora și a minimiza, deci, dozajul în timpul tratamentului”, a declarat Desrosiers. „O altă caracteristică impresionantă a acestor nanotransportori este că pot fi direcționați, targetați către anumite părți ale organismului unde este vital ca medicamentul să fie prezent – iar acest lucru, în principiu, ar trebui să reducă incidența majorității efectelor secundare”. Pentru a demonstra eficacitatea și viabilitatea acestor nanotransportori, cercetătorii au făcut echipă cu mai mulți biochimiști. Utilizând transportorul de medicamente specific pentru doxorubicină, echipa a demonstrat că o formulă specifică, clară de transport al medicamentelor permite menținerea doxorubicinei în sânge și în același timp va reduce drastic difuzia acesteia spre alte organe, cum ar fi inima, plămânii și pancreasul.
La șoarecii tratați cu această formulă, doxorubicina a fost menținută de 18 ori mai mult timp în sânge și cardiotoxicitatea sa a fost, de asemenea, mult redusă – șoarecii au fost menținuți mult mai sănătoși, crescând normal în greutate. „O altă mare proprietate a nanotransportorilor pare-se că este și versatilitatea”, a declarat un cercetător. „Deocamdată, am reușit să demonstrăm cu succes principiul de funcționare al acestor nanotransportori pentru două medicamente diferite. Dar, datorită gradului ridicat de programabilitate a chimiei ADN-ului și proteinelor, acum se pot proiecta acești transportori pentru a livra cu precizie o gamă largă de molecule terapeutice”. A mai adăugat că: „În plus, acești transportori ar putea fi, de asemenea, combinați chiar și cu transportori liposomici realizați de oameni, care acum sunt folosiți pentru a livra medicamente, dar la viteze diferite”.
Cercetătorii sunt acum nerăbdători să valideze eficiența clinică a descoperirii lor și, în primul rând, având în vedere că nanotransportorul de doxorubicină este programat să mențină în mod optim medicamentul în circulația sanguină, acesta ar putea fi utilizat pentru tratarea cancerelor de sânge (a leucemiilor). „Ne imaginăm că nanotransportori similari ar putea fi, de asemenea, dezvoltați pentru a livra medicamente în alte locații specifice din organism, dar și pentru a reuși să maximizăm prezența medicamentului în zonele tumorale”, a declarat Vallée-Bélisle. „Acest lucru ar îmbunătăți semnificativ eficiența medicamentelor, scăzând, în același timp, incidența efectelor secundare asociate medicamentației”.
