Primul pas în alegerea tratamentului cel mai potrivit, adecvat și personalizat, pentru un pacient bolnav de cancer, îl reprezintă identificarea exactă, strictă a tipului specific de cancer, inclusiv „a epicentrului” bolii, adică a locului primar (organul sau o anumită parte a corpului) de unde a început procesul patologic. În cazuri destul de rare, originea unui astfel de proces nu poate fi determinată (nici măcar cu marjă de eroare), chiar și cu ajutorul unor teste extinse și complexe. Deși aceste tipuri de cancer cu localizare primară necunoscută au tendința de a fi agresive și sunt greu de gestionat, oncologii trebuie să le trateze cu terapii care nu sunt țintite, frecvent toxice chiar și pentru pacient și care, din păcate, au rate mici de reușită. În ultimii ani, se caută alternative mult mai benefice față de chimioterapia care afectează o mare parte din celule sănătoase ale pacienților bolnavi de cancer.
O nouă abordare în domeniul învățării profunde (deep-learning), dezvoltată de cercetătorii de la Koch Institute for Integrative Cancer Research din cadrul MIT și din cadrul Massachusetts General Hospital (MGH) ar putea ajuta la clasificarea cancerelor ale căror origine primară este necunoscută, prin analiza aprofundată a programelor de expresie genică legat de dezvoltarea și diferențierea celulară timpurie. Studiul a fost publicat pe data de 30 august 2022, într-o revistă de domeniu renumită. „Uneori poți să aplici toate instrumentele și protocoalele pe care le ai la dispoziție, și tot nu reușești să obții un răspuns viabil”, a afirmat Salis Garg, cercetător clinic. „Instrumentele de învățare automată, precum acesta, ar putea să le dea posibilitatea oncologilor de a alege tratamente mult mai eficiente și personalizabile în funcție de nevoile pacientului, deoarece fiecare dintre noi este o individualitate biologică unică”.
Garg este autorul principal al studiului publicat în revista Cancer Discovery. Instrumentul de învățare profundă, care se bazează, bineînțeles, pe principiile inteligenței artificiale, poate să identifice diferite tipuri de cancer cu un grad ridicat de acuratețe și sensibilitate. Învățarea automată (machine-learning), reprezintă o subdisciplină a inteligenței artificiale în care programele de calculator (algoritmii) învață asociații cu capacitate de predicție, analizând exemplele date. Învățarea automată este, pe scurt, aplicarea de modele statistice, rezultate în urma analizei datelor, cu ajutorul calculatoarelor. Aceasta utilizează un set larg de tehnici de statistică, analizând rezultate deja existente, spre deosebire de învățarea profundă (deep learning) care se bazează pe modele autentice, cu mai puține date preexistente, subiacente și care, prin urmare, este capabilă să gestioneze date mult mai complexe.
Învățarea automată și aplicabilitatea acesteia în domeniul clinic
Analiza diferențelor de expresie a genelor între diferitele tipuri de tumori cu origine primară necunoscută este o problemă care poate fi cu ușurință (și cu o precizie uimitoare) rezolvată de către mecanismele de învățare automată. În esență, celulele canceroase au o structură specifică, diferită față de celulele normale; de asemenea, se comportă și diferit, au un metabolism propriu și se divid mult mai rapid decât celulele normale, în mare parte din cauza modificărilor extinse ale modului în care sunt exprimate genele lor. Datorită progreselor înregistrate în proliferarea celulelor unice și a eforturilor de a cataloga diferite modele specifice de expresie celulară, sunt disponibile o mulțime de date care descriu modul în care, deci cum, și de unde, apar diferitele tipuri de cancer.
Cu toate acestea, construirea unui model de învățare automată care să poată aprecia diferențele dintre celulele sănătoase, normale, și cele tumorale, existente în diferitele tipuri de cancer, într-un instrument practic de diagnosticare, presupune a lua în considerare o gamă extrem de mare de variabile care ar putea justifica succesul sau eșecul muncii depuse: dacă un model este prea complex și ia în calcul mult prea multe caracteristici privitoare la expresia genelor canceroase, modelul poate părea că va identifica, cu fidelitate, alte tipuri de cancer cu același tip de expresie a genelor, însă se poate dovedi deficitar când vine vorba de a întâlni date noi (deci alte tipuri de cancer). Cu toate acestea, prin simplificarea modelului și reducerea numărului de variabile, caracteristice introduse (deci, dacă este prea simplu), modelul poate rata, de fapt, exact acele informații care ar putea duce la clasificarea viabilă ale anumitor tipuri de cancer.
Pentru a găsi un echilibru între reducerea numărului de caracteristici și extragerea, în același timp, a celor mai relevante informații și date, echipa a concentrat modelul asupra unui proces fiziologic normal în dinamica apariției cancerului: analiza semnelor clare care indică alterarea căilor de dezvoltare a celulelor canceroase. Spre exemplu, pe măsură ce un embrion se dezvoltă și celulele nediferențiate se specializează în diverse organe, o multitudine de căi direcționează modul în care celulele se divid, cresc, își schimbă forma, se specializează și, în cele din urmă, migrează. Pe măsură ce tumora se dezvoltă, celulele canceroase pierd multe dintre trăsăturile specializate ale unei celule mature, adulte. În același timp, ele încep să semene, într-o oarecare măsură, cu celulele embrionare: capătă capacitatea de a prolifera, de a se transforma și, implicit, de a da metastaze în noi țesuturi.
Se știe, de asemenea, că multe dintre programele de expresie genetică ce conduc embriogeneza sunt reactivate sau dereglate în celulele canceroase, de unde și apariția procesului patologic. Cercetătorii au comparat două atlase celulare mari, identificând astfel corelații între tumori și celulele embrionare: The Cancer Genome Atlas Program (TCGA), care conține date privitoare la expresia genetică pentru 33 de tipuri de tumori și Mouse Organogenesis Cell Atlas (MOCA), care prezintă 56 de traiectorii diferite, separate, ale celulelor embrionare, pe măsură ce acestea se dezvoltă, se diferențiază, se specializează și proliferează într-o anumită direcție funcțională. „Instrumentele de rezoluție a celulelor unice au schimbat semnificativ modul în care putem studia biologia și fiziologia cancerului (…), iar odată cu apariția atlaselor de celule embrionare, în special a celor care se concentrează pe fazele timpurii ale organogenezei, cum ar fi MOCA, putem extinde instrumentele noastre dincolo de informațiile histologice și genomice, astfel încât să dăm undă verde noilor modalități de identificare a tumorilor și de dezvoltare de noi tratamente”.
Rezultatul echipei de cercetători este reprezentat de „o hartă” a corelațiilor specifice, stricte, dintre modelele de expresie genetică întâlnite în diferite tipuri de tumori și modelele întâlnite în celulele embrionare fiziologic normale. Ulterior, harta a fost transformată într-un model de învățare automată. Cercetătorii au împărțit expresia genică a probelor de tumori din TCGA în componente individuale care corespund unui anumit model în dinamica de dezvoltare și, apoi, au atribuit fiecăreia dintre aceste componente o valoare matematică. După aceea, cercetătorii au construit un model de învățare automată numit Developmental Multilayer Perceptron (D-MLP), care acordă un anumit „punctaj” unei tumori în funcție de caracteristicile de dezvoltare identificate (pe baza rezultatelor deja introduse și a altor tipuri de analize specifice domeniului oncologic), și apoi îi prezice stadiul dar, mai presus de toate, originea, punctul primar în care a început dezvoltarea patologiei.
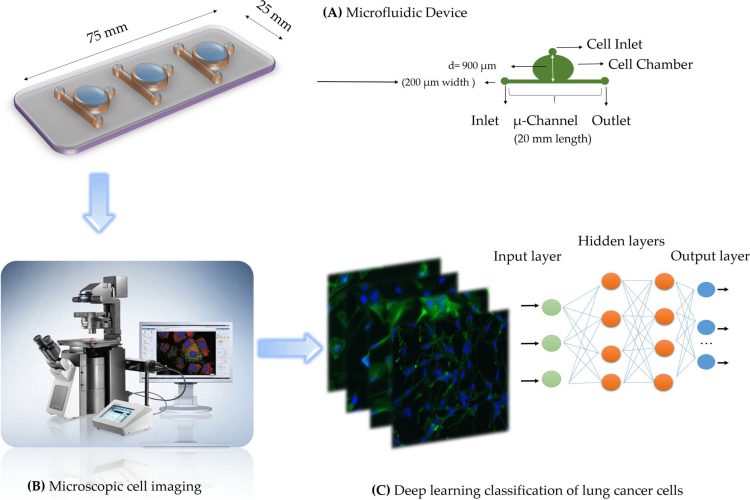
Clasificarea tipurilor de tumori prin utilizarea învățării automate
După ce modelul a fost punct la punct și „învățat” (prin introducerea unui număr mare de date provenite de la cazuri clinice anterioare), instrumentul D-MLP a fost aplicat la nu mai puțin de 52 de noi eșantioane de cancer deosebit de dificile, de origine primară necunoscută, care nu au putut fi diagnosticate exact cu ajutorul instrumentelor și protocoalelor de oncologie avute de către medici la dispoziție. Aceste cazuri au fost considerate, de fapt, cele mai dificile cazuri observate la MGH de-a lungul unei perioade de 4 ani, începând cu anul 2017. Revoluționar a fost faptul că modelul D-MLP a clasificat tumorile în 4 categorii și a livrat predicții și informații viabile care ar putea permite, în sfârșit, un diagnostic fix și posibilitatea de a oferi pacienților un tratament specific.
Spre exemplu, un eșantion de probe a provenit de la o pacientă cu antecedente de cancer mamar, care a prezentat semne de cancer agresiv la nivelul organelor abdominale. Inițial, oncologii nu au putut identifica o masă tumorală evidentă și, astfel, nu au putut clasifica celulele tumorale cu ajutorul instrumentelor de care dispuneau la momentul respectiv. Acum, cu ajutorul D-MLP, instrumentul a livrat date conform cărora pacienta ar suferi de cancer ovarian în primă fază. La șase luni de la analiza probelor și primirea rezultatelor, a fost observat faptul că, într-adevăr, pacienta prezintă o urmă de masă tumorală la nivelul ovarelor, ceea ce a reprezentat însăși originea tumorii mamare. Mai mult decât atât, comparațiile sistematice dintre celulele tumorale și cele embrionare au dezvăluit informații promițătoare și chiar surprinzătoare privitoare la profilurile de expresie genetică ale anumitor tipuri de tumori.
De exemplu, în stadiile timpurii ale dezvoltării embrionare, are loc formarea unui tub intestinal rudimentar, plămânii și alte organe din apropiere provenind din intestinul anterior, iar cea mai mare parte a tractului digestiv se formează din intestinul mijlociu și posterior. Studiul a arătat că celulele tumorale derivate din plămâni au prezentat asemănări puternice nu doar cu intestinul anterior (așa cum, bineînțeles, ar fi de așteptat, din moment ce la începuturi se formează din aceasta), ci și cu traiectoriile de dezvoltare derivate din intestinul mijlociu și posterior. În acest caz, descoperirile sugerează că diferențele dintre programele de dezvoltare ar putea fi deschide noi direcții de exploatare în domeniul terapeutic, în același mod în care mutațiile genetice sunt utilizate, în ziua de astăzi, pentru a concepe tratamente personalizate sau țintite pentru cancer.
Deși instrumentul de diagnosticare D-MLP pare destul de convingător, util și fiabil în practica clinică, în special în ceea ce privește clasificarea și diagnosticarea originii tumorilor, acesta are și unele limitări care s-ar putea dovedi critice. În viitor, echipa de cercetători intenționează, așa cum era de așteptat, să îmbunătățească și mai mult puterea de predicție a modelului lor bazat pe învățarea automată, prin încorporarea altor tipuri de date, în special a informațiilor obținute din protocoale de radiologie, microscopie și alte tipuri de imagistică nucleară. „După părerea noastră, expresia genetică din timpul dezvoltării celulelor reprezintă doar o mică parte din toți factorii care ar putea fi utilizați cu încredere pentru a diagnostica și trata cancerele”, a afirmat Garg. „Integrarea la un loc a informațiilor de radiologie, patologie și expresie genetică ar putea reprezenta adevăratul pas semnificativ în direcția dezvoltării medicinei personalizate pentru pacienții care suferă de cancer”.